Du möchtest verstehen, was Tumormarker sind, wie sie in der medizinischen Diagnostik eingesetzt werden und welche Rolle sie bei der Krebsbehandlung spielen? Dieser Text richtet sich an Patienten, Angehörige sowie medizinisch Interessierte, die fundierte und präzise Informationen über diese wichtigen diagnostischen Werkzeuge suchen, um die Bedeutung von Tumormarkern für die Früherkennung, Diagnose und Überwachung von Krebserkrankungen zu erfassen.
Was sind Tumormarker und wie funktionieren sie?
Tumormarker sind Substanzen, die im Körper vorkommen und bei der Anwesenheit bestimmter Krebsarten erhöht sein können. Sie können im Blut, Urin, Stuhl oder in Gewebeproben nachgewiesen werden. Es ist wichtig zu verstehen, dass Tumormarker nicht spezifisch für Krebs sind; erhöhte Werte können auch bei gutartigen Erkrankungen auftreten. Ihre Hauptbedeutung liegt in der Kombination mit anderen diagnostischen Verfahren wie bildgebenden Verfahren (z.B. Ultraschall, CT, MRT) und Biopsien. Tumormarker können entweder vom Tumor selbst produziert werden (z.B. Hormone oder Enzyme) oder eine Reaktion des Körpers auf den Tumor sein (z.B. bestimmte Antigene). Die Messung von Tumormarkern erfolgt meist über Blutuntersuchungen in einem Labor.
Anwendungsgebiete von Tumormarkern in der Medizin
Die Anwendungsbereiche von Tumormarkern in der Medizin sind vielfältig und umfassen verschiedene Phasen des Krankheitsmanagements. Ihre primäre Funktion ist nicht immer die alleinige Krebsdiagnose, sondern vielmehr die Unterstützung bei folgenden Prozessen:
- Früherkennung: In einigen Fällen können Tumormarker Hinweise auf eine Krebserkrankung liefern, bevor Symptome auftreten. Dies ist besonders relevant für Personen mit einem erhöhten familiären Risiko. Die Früherkennung ermöglicht eine potenziell frühere und damit oft erfolgreichere Behandlung.
- Diagnoseunterstützung: Tumormarker können helfen, den Verdacht auf Krebs zu erhärten oder bestimmte Krebsarten zu identifizieren, insbesondere wenn Symptome vorliegen, die auf verschiedene Ursachen hindeuten könnten. Sie dienen als Ergänzung zu bildgebenden und histologischen Untersuchungen.
- Verlaufs- und Therapiekontrolle: Während einer Krebstherapie werden Tumormarker regelmäßig überwacht. Ein Anstieg der Werte kann auf ein Fortschreiten der Erkrankung oder eine Resistenz gegenüber der Therapie hinweisen, während ein Abfall oft eine erfolgreiche Behandlung signalisiert. Dies ermöglicht eine frühzeitige Anpassung der Behandlungsstrategie.
- Rezidiv-Früherkennung: Nach erfolgreicher Behandlung können Tumormarker zur Überwachung eingesetzt werden, um ein Wiederauftreten des Krebses (Rezidiv) frühzeitig zu erkennen, oft bevor klinische Symptome auftreten.
- Prognoseabschätzung: Bestimmte Tumormarker können Hinweise auf die Aggressivität eines Tumors und die voraussichtliche Prognose geben.
Wichtige Tumormarker und ihre Zuordnung
Es gibt eine Vielzahl von Tumormarkern, die für unterschiedliche Krebsarten relevant sind. Die Kenntnis der spezifischen Marker und ihrer Zuordnungen ist essenziell für eine gezielte Diagnostik und Therapieüberwachung. Hier ist eine Übersicht über einige der bekanntesten und am häufigsten verwendeten Tumormarker:
| Tumormarker (Abkürzung) | Hauptindikationen | Typische Tumore | Besonderheiten |
|---|---|---|---|
| Prostata-spezifisches Antigen (PSA) | Verdacht auf Prostatakrebs, Verlaufs- und Therapiekontrolle | Prostatakarzinom | Kann auch bei gutartigen Prostataerkrankungen (z.B. Entzündung, gutartige Vergrößerung) erhöht sein. |
| Carcinoembryonales Antigen (CEA) | Krebs der Verdauungsorgane, Lunge, Brust; Verlaufs- und Therapiekontrolle | Kolonkarzinom, Magenkarzinom, Lungenkarzinom, Mammakarzinom, Pankreaskarzinom, Leberzellkarzinom | Unscharfer Marker, der auch bei Entzündungen und anderen gutartigen Erkrankungen erhöht sein kann. |
| Klassischer Alpha-Fetoprotein (AFP) | Leberzellkarzinom, Keimzelltumoren (Hoden-, Eierstockkrebs) | Hepatozelluläres Karzinom, Seminom, Nicht-Seminom-Tumoren (z.B. Chorionkarzinom) | Kann auch bei schweren Lebererkrankungen wie Zirrhose erhöht sein. |
| Klassischer Krebs-Antigen 19-9 (CA 19-9) | Tumore des Verdauungstrakts, insbesondere der Gallenwege und Bauchspeicheldrüse | Pankreaskarzinom, Gallenwegskarzinom, Magenkarzinom, Kolonkarzinom | Kann auch bei gutartigen Erkrankungen des Verdauungstrakts (z.B. Gallenblasenentzündung, Bauchspeicheldrüsenentzündung) erhöht sein. |
| Klassischer Krebs-Antigen 125 (CA 125) | Eierstockkrebs, Verlaufs- und Therapiekontrolle | Ovarialkarzinom | Kann auch bei gutartigen gynäkologischen Erkrankungen (z.B. Endometriose, Myome, Beckenentzündungen) oder anderen abdominellen Prozessen erhöht sein. |
| Hormone (z.B. β-hCG) | Bestimmte Keimzelltumoren, Schwangerschaftskomplikationen | Chorionkarzinom, bestimmte Formen von Hodenkrebs, Gestations-Trophoblastentumoren | Erwartungsgemäß erhöht in der Schwangerschaft. |
| Procalcitonin (PCT) | Indikator für bakterielle Infektionen und Sepsis, kann in Zusammenhang mit Krebs zur Beurteilung des Allgemeinzustandes relevant sein | Obwohl kein direkter Tumormarker, ist es wichtig bei der Beurteilung von Patienten mit Krebserkrankungen, die zu Infektionen neigen. | Deutlich erhöhte Werte weisen oft auf eine bakterielle Infektion hin. |
Herausforderungen und Limitationen von Tumormarkern
Trotz ihrer Nützlichkeit sind Tumormarker nicht unumstritten und haben klare Limitationen, die bei ihrer Interpretation berücksichtigt werden müssen. Eine alleinige Diagnose oder ein Ausschluss von Krebs allein auf Basis von Tumormarkerwerten ist in den meisten Fällen nicht möglich.
- Spezifität: Viele Tumormarker sind nicht spezifisch genug. Das bedeutet, dass erhöhte Werte auch bei gutartigen Erkrankungen, Entzündungen, Infektionen oder sogar nach bestimmten medizinischen Eingriffen auftreten können. Dies kann zu falsch positiven Ergebnissen führen und unnötige Ängste oder weitere Untersuchungen verursachen.
- Sensitivität: Umgekehrt können Tumormarker in frühen Stadien einer Krebserkrankung oder bei bestimmten Tumorarten niedrig oder sogar normal sein. Dies kann zu falsch negativen Ergebnissen führen, bei denen eine Krebserkrankung übersehen wird, obwohl sie vorhanden ist.
- Standardisierung: Die Ergebnisse von Tumormarker-Tests können je nach Labor, Testmethode und verwendeter Reagenzien variieren. Dies erschwert den Vergleich von Ergebnissen zwischen verschiedenen Laboren oder über die Zeit hinweg, wenn nicht dieselben Methoden verwendet werden.
- Individuelle Variationen: Es gibt natürliche Schwankungen in den Tumormarkerwerten zwischen verschiedenen Individuen, auch bei gesunden Personen. Was für den einen ein normaler Wert ist, kann für den anderen leicht erhöht sein.
- Therapie-Monitoring: Während Tumormarker bei der Therapiekontrolle hilfreich sein können, ist es wichtig zu beachten, dass sie nicht immer die klinische Antwort auf eine Therapie exakt widerspiegeln. Ein stabiler oder leicht erhöhter Tumormarkerwert bedeutet nicht zwangsläufig, dass die Behandlung nicht wirksam ist, und ein sinkender Wert kann auch auf andere Faktoren zurückzuführen sein.
Die Interpretation von Tumormarkerwerten sollte daher immer im Kontext des gesamten klinischen Bildes erfolgen, einschließlich der Krankengeschichte, der Symptome, der Ergebnisse bildgebender Verfahren und anderer Laboruntersuchungen. Ein erfahrener Arzt wird diese Informationen integrieren, um eine fundierte Entscheidung zu treffen.
Wie werden Tumormarker bestimmt?
Die Bestimmung von Tumormarkern erfolgt in der Regel durch standardisierte Laboruntersuchungen. Der gängigste Weg ist die Analyse einer Blutprobe. Der Prozess umfasst dabei mehrere Schritte:
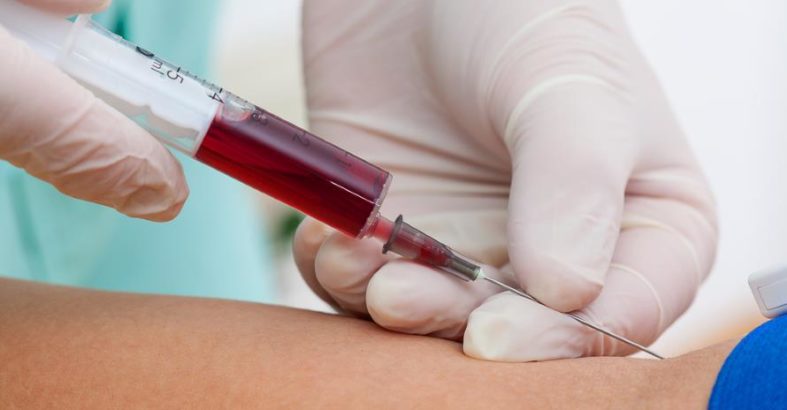
- Blutentnahme: Eine medizinische Fachkraft entnimmt eine Blutprobe, meist aus einer Vene am Arm, unter sterilen Bedingungen.
- Probenvorbereitung: Das Blut wird in ein Labor gesendet, wo es weiterverarbeitet wird. Oft wird das Blutserum oder Plasma benötigt, d.h. die flüssigen Bestandteile des Blutes, nachdem die festen Blutzellen abgetrennt wurden.
- Laboranalyse: Mithilfe spezifischer immunologischer oder enzymatischer Nachweisverfahren (z.B. ELISA – Enzyme-linked Immunosorbent Assay, oder CLIA – Chemiluminescent Immunoassay) wird die Konzentration des gesuchten Tumormarkers im Serum oder Plasma bestimmt. Diese Verfahren sind darauf ausgelegt, den Marker sehr empfindlich und spezifisch nachzuweisen.
- Ergebnisbewertung: Die ermittelte Konzentration wird mit Referenzbereichen verglichen. Diese Referenzbereiche geben die typischen Werte bei gesunden Personen an. Überschreitet der gemessene Wert den oberen Referenzbereich, kann dies auf eine Anomalie hinweisen.
Neben Blutproben können Tumormarker auch in anderen Körperflüssigkeiten wie Urin (z.B. für Blasenkrebsmarker wie NMP22) oder Stuhl (z.B. für okkultes Blut als Hinweis auf Darmkrebs) sowie in Gewebeproben (z.B. Biopsien) nachgewiesen werden. Die Wahl der Probe hängt vom Verdacht auf eine bestimmte Krebsart und dem spezifischen Marker ab.
Regelmäßige Vorsorge und Tumormarker
Die Rolle von Tumormarkern in der allgemeinen Krebsvorsorge ist ein komplexes Thema und variiert je nach Krebsart und Empfehlung der medizinischen Fachgesellschaften. Während einige Tumormarker bei der Früherkennung spezifischer Krebsarten eine Rolle spielen können, werden sie selten als alleiniger Test für eine breite Bevölkerungsuntersuchung eingesetzt.
- PSA und Prostatakrebs: Der PSA-Wert wird bei Männern zur Früherkennung von Prostatakrebs eingesetzt. Die Empfehlungen zur PSA-Vorsorge sind jedoch umstritten, da PSA auch bei gutartigen Erkrankungen erhöht sein kann und die Früherkennung nicht immer zu besseren Behandlungsergebnissen führt, sondern auch zu Überdiagnosen und Übertherapien. Eine individuelle Beratung mit dem Arzt ist hier essenziell.
- Koloskopie als Goldstandard: Für die Früherkennung von Darmkrebs ist die Koloskopie die etablierte Methode. Stuhltests auf okkultes Blut können als ergänzende Screening-Maßnahme dienen, sind aber weniger sensitiv und spezifisch als die Koloskopie. CEA wird hier eher zur Verlaufs- und Therapiekontrolle nach einer Darmkrebserkrankung eingesetzt.
- Gynäkologische Vorsorge: Bei Frauen ist die regelmäßige gynäkologische Untersuchung und der PAP-Abstrich (Zytologie) zur Früherkennung von Gebärmutterhalskrebs Standard. CA 125 wird primär zur Verlaufs- und Therapiekontrolle bei bekanntem Eierstockkrebs eingesetzt und nicht routinemäßig zur Früherkennung in der Allgemeinbevölkerung, da seine Spezifität für Eierstockkrebs begrenzt ist.
- Andere Krebsarten: Für viele andere Krebsarten gibt es derzeit keine etablierten Tumormarker-basierten Vorsorgeuntersuchungen für die breite Bevölkerung. AFP kann bei Personen mit chronischen Lebererkrankungen zur Überwachung des Risikos auf Leberzellkarzinom eingesetzt werden.
Generell gilt, dass eine gesunde Lebensweise mit ausgewogener Ernährung, regelmäßiger Bewegung und dem Verzicht auf Rauchen und übermäßigen Alkoholkonsum die wichtigste Säule der Krebsprävention darstellt. Bei familiärer Vorbelastung oder spezifischen Risikofaktoren ist eine individuelle Beratung durch den Arzt zur Teilnahme an Früherkennungsprogrammen ratsam.
Entwicklungen und Zukunftsperspektiven bei Tumormarkern
Die Forschung im Bereich der Tumormarker ist dynamisch und zielt darauf ab, die Genauigkeit, Spezifität und Anwendbarkeit dieser diagnostischen Werkzeuge zu verbessern. Neue Technologien und ein tieferes Verständnis der Tumorentstehung eröffnen vielversprechende Perspektiven:
- Multimarker-Tests: Anstatt sich auf einzelne Marker zu verlassen, werden zunehmend Tests entwickelt, die eine Kombination aus mehreren Tumormarkern analysieren. Die gleichzeitige Messung verschiedener Substanzen kann die diagnostische Genauigkeit erhöhen und die Differenzierung zwischen gutartigen und bösartigen Erkrankungen verbessern.
- Flüssigbiopsien (Liquid Biopsies): Ein besonders spannendes Feld sind die sogenannten Flüssigbiopsien. Diese Analysen suchen nach zirkulierenden Tumor-DNA (ctDNA), zirkulierenden Tumor-Zellen (CTCs) oder anderen Molekülen, die vom Tumor in den Blutkreislauf abgegeben werden. Flüssigbiopsien haben das Potenzial, nicht-invasive Früherkennung, Überwachung des Therapieansprechens und die Detektion von minimaler Resterkrankung zu revolutionieren.
- Epigenetische Marker: Veränderungen in der Genexpression ohne Veränderungen in der DNA-Sequenz (epigenetische Veränderungen) spielen bei Krebs eine wichtige Rolle. Die Untersuchung von DNA-Methylierungsmustern oder miRNA-Profilen im Blut könnte zukünftig als sensitive und spezifische Marker für verschiedene Krebsarten dienen.
- Künstliche Intelligenz (KI) und maschinelles Lernen: KI-Algorithmen werden eingesetzt, um große Datensätze von Tumormarkerwerten und anderen klinischen Daten zu analysieren. Dies kann helfen, komplexe Muster zu erkennen, die für das menschliche Auge nicht offensichtlich sind, und so die Genauigkeit von Diagnosen und Prognosen zu verbessern.
- Personalisierte Medizin: Mit fortschreitendem Verständnis der molekularen Grundlagen einzelner Tumore werden zukünftig noch spezifischere Tumormarker für die personalisierte Therapie und Überwachung entwickelt werden können. Dies ermöglicht eine noch gezieltere und effektivere Behandlung, die auf die individuellen Charakteristika des Tumors und des Patienten zugeschnitten ist.
FAQ – Häufig gestellte Fragen zu Tumormarker in der Medizin
Was bedeutet ein erhöhter Tumormarker-Wert?
Ein erhöhter Tumormarker-Wert bedeutet nicht automatisch, dass Sie Krebs haben. Er kann auf eine Vielzahl von Zuständen hinweisen, darunter gutartige Erkrankungen, Entzündungen oder Infektionen. Es ist ein Hinweis, der weiter untersucht werden muss. Ihr Arzt wird diesen Wert im Kontext Ihrer gesamten gesundheitlichen Situation beurteilen.
Kann ein Tumormarker Krebs ausschließen?
Nein, ein normaler Tumormarker-Wert kann Krebs nicht vollständig ausschließen. In frühen Stadien einer Krebserkrankung oder bei bestimmten Tumorarten können die Tumormarkerwerte im Normbereich liegen. Daher sind weitere diagnostische Maßnahmen wie bildgebende Verfahren und ggf. eine Biopsie unerlässlich.
Wie oft sollten Tumormarker kontrolliert werden?
Die Häufigkeit der Tumormarker-Kontrollen hängt von der individuellen Situation ab. Sie wird von Ihrem behandelnden Arzt festgelegt, basierend auf der Krebsart, dem Stadium der Erkrankung, der Art der Behandlung und ob die Kontrolle zur Früherkennung, Diagnoseunterstützung oder zur Therapiekontrolle dient.
Welcher Tumormarker ist der beste?
Es gibt nicht DEN einen besten Tumormarker. Jeder Marker ist spezifisch für bestimmte Krebsarten und hat seine eigenen Stärken und Schwächen. Die Wahl des relevanten Markers hängt vom klinischen Verdacht und der Art der vermuteten Erkrankung ab. Oft ist eine Kombination von Markern oder die Kombination mit anderen diagnostischen Methoden am aussagekräftigsten.
Sind Tumormarker schädlich?
Die Bestimmung von Tumormarkern ist in der Regel nicht schädlich. Die häufigste Methode ist die Blutentnahme, die ein routinemäßiges und sicheres medizinisches Verfahren darstellt. Es gibt keine bekannten schädlichen Effekte durch die Messung selbst.
Können Tumormarker vorhersagen, wie schnell ein Krebs wächst?
Manche Tumormarker können Hinweise auf die Aggressivität eines Tumors und damit indirekt auf die Wachstumsgeschwindigkeit geben. Allerdings ist dies nicht bei allen Markern der Fall, und die Interpretation erfordert Fachwissen. Die Bestimmung der Wachstumsgeschwindigkeit erfolgt oft durch eine Kombination aus Tumormarkerwerten, bildgebenden Verfahren und der histologischen Untersuchung des Tumorgewebes.
Was ist der Unterschied zwischen einem Tumormarker und einem Biomarker?
Tumormarker sind eine Unterkategorie von Biomarkern. Ein Biomarker ist allgemein eine Substanz, die objektiv gemessen werden kann und Hinweise auf einen biologischen Zustand gibt. Tumormarker sind spezifisch Biomarker, die mit dem Vorhandensein oder der Entwicklung einer Krebserkrankung assoziiert sind.